
01炒股资金配资
前言
卵圆孔是胚胎时期心房间隔的原发隔和继发隔未完全融合所遗留的裂隙样通道,出生后逐渐闭合,3岁以上仍未闭合称之为卵圆孔未闭(patent foramen ovale,PFO),成人PFO发生率约为20%-34%。近年来,随着对PFO研究的不断深入,发现其特殊的解剖结构易于(条件性)介导血液从右向左分流(right-to-left shunt,RLS),与一些疾病相关,形成PFO相关综合征,包括PFO相关性卒中(patent foramen oval-associated stroke,PFO-AS)和PFO相关非卒中性疾病(patent foramen oval related nonapoplectic disease,PFO-NAD),如偏头痛、减压病、斜卧呼吸-直立性低氧血症和系统栓塞等。近年,国内外在不同领域发表了PFO相关的共识或指南,但主要集中在PFO-AS的处理。对于PFO-NAD,虽有一些共识和建议,但由于循证医学证据有限,临床医生常常根据观察性研究结果作为介入治疗的依据,有一定的盲目性。
为更好指导我国医师的临床实践,中国人体健康科技促进会结构性心脏病专委会和中国医师协会神经内科分会组织国内结构性心脏病、神经科和超声影像科等相关学科专家,制定了《卵圆孔未闭相关非卒中性疾病防治中国专家共识》。
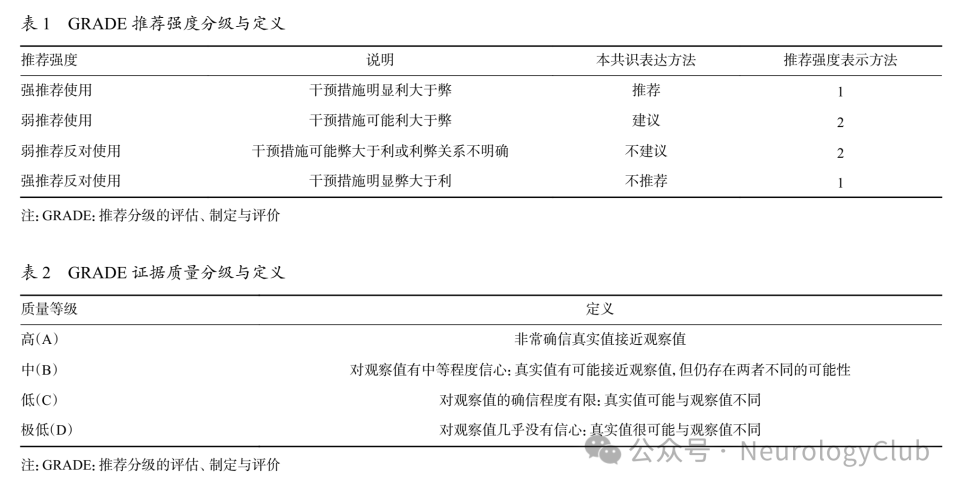
本共识涉及的疾病除偏头痛外,多数为临床上发病率偏低、患者群体较小的疾病,同时目前针对PFO-NAD的临床研究尤其是高质量随机对照临床研究较少。本共识证据和推荐意见的评价方法采用推荐分级的评估、制定与评价(Grading of Recommendations Assessment,Development and Evaluation,GRADE)分级系统,见表1和表2。

02
偏头痛
偏头痛(migraine)是最常见的原发性头痛之一,其临床表现为反复发作、搏动性中重度头痛,头痛部位单侧或双侧均可发生,可伴有恶心、呕吐、畏光、畏声。约14%的偏头痛患者发作前可出现局灶性神经功能缺损即先兆症状,其中以视觉先兆最为常见,此外也包括感觉先兆,运动先兆等,先兆症状多于头痛前出现,也可与头痛伴随。大约10%偏头痛患者为有先兆偏头痛(migraine with aura,MA),80%偏头痛患者为无先兆偏头痛(migraine without aura,MwoA),部分患者为两者的混合型。
我国的偏头痛年患病率为9.3%,世界卫生组织将偏头痛列为第二大失能性疾病,是导致50岁以下人群失能的最主要原因,其所致的失能超过所有其他神经系统疾病产生疾病负担的总和。然而,偏头痛的发病机制目前尚未完全明确,近年来研究发现RLS与偏头痛存在着密切的相关性。
2.1 PFO引起偏头痛的机制与假说
2.1.1 微栓子假说
当PFO引起心房水平出现RLS时,静脉系统内形成的微血栓进入左心房,随动脉血进入大脑,导致局部脑组织灌注不足,引起短暂性缺氧,诱发皮层扩散性抑制(cortical spreading depression,CSD),引发偏头痛。微血栓引起的局部脑组织灌注不足,更易发生于后循环,比如枕叶皮质。相关功能部位的低灌注易引起视觉先兆,这与PFO相关性偏头痛中的MA更常见相一致。CSD动物模型也证实,空气微栓塞引起短暂的低灌注,可触发CSD。中国医学科学院阜外医院利用光学相干断层扫描技术(optical coherence tomography,OCT),在偏头痛合并PFO的患者中发现,PFO内原位血栓发生率为12.2%。西安交通大学第一附属医院发PFO偏头痛患者枕叶皮层兴奋性高,对光刺激更为敏感。
2.1.2 致头痛因子分流
当PFO引起RLS时,静脉血中的某些可能诱发偏头痛的物质,如5-羟色胺、一氧化氮、降钙素基因相关肽等,未经过肺循环代谢降解而直接进入动脉系统,除引起脑动脉扩张外,还可直接刺激三叉神经,引起偏头痛发作。有证据表明,PFO封堵术后患者随访期间外周血5-羟色胺水平降低27.27%,与仅用单纯药物治疗者差异有统计学意义(P=0.0034)。
2.1.3 脑血流自动调节功能异常
在血压波动范围内,脑灌注可通过自动调节血管的收缩和扩张维持在一个相对稳定的水平。Guo等证实,与无RLS的偏头痛患者相比,RLS患者的脑血流速度和自动调节指数明显降低,提示脑血流自动调节功能受损,可能是联系偏头痛和RLS的潜在机制。
2.1.4 遗传因素
编码基因参与心脏发育的结构蛋白和转录因子的基因突变可能在一些PFO合并偏头痛的遗传过程中发挥作用。2004年,Wilmshurst等首次提出PFO和偏头痛可能有共同的遗传基础。随后,2010年的一项meta分析研究了MTHFR基因中的C677T多态性和ACE基因中的I/D多态性是否与偏头痛相关,结果显示MTHFR677TT基因型与MA风险的增加相关。Szczygiol等发现PFO在MTHFR纯合隐性基因型MA患者中的患病率显著增加,提示PFO和偏头痛可能有共同的遗传基础。
2.1.5 血小板激活
PFO对血流的剪切力可激活血小板,使血小板释放活性代谢产物,引起偏头痛发作。LEARNER研究发现,与健康人相比,MA患者具有更高的促血栓表型和氧化应激改变,应用P2Y12受体拮抗剂作用可缓解偏头痛。CANOA研究亦发现氯吡格雷可减少房间隔缺损(atrial septal defect,ASD)封堵后新发偏头痛。
2.2 PFO和偏头痛之间的争议
2.2.1 PFO和偏头痛是否有关
PFO与偏头痛之间的因果关系仍存在较大争议。早在1998年DelSette等进行了一项病例对照研究,显示MA患者RLS率为41%,而正常对照组为16%(P<0.005),首次提出偏头痛和PFO之间可能存在直接相关性。此后,基于偏头痛和PFO之间进行了大量研究。MA患者PFO发生率41%-57%,我国的一项多中心研究也显示,PFO的发生率在MA组为63.75%。
PFO解剖特征与MA有关。MA患者中PFO合并房间隔瘤(atrial septal aneurysms,ASA)发生率较高、PFO直径较大。MA发作的严重程度和频率与对比增强经颅多普勒超声(contrast-enhanced transcranial doppler,cTCD)检测到的微气泡数量相关。还有研究证明,RLS与MA发病年龄有关,RLS越严重或PFO合并ASA,MA发病年龄越早。然而,也有研究认为PFO与MA无关,年龄越大,PFO和偏头痛之间的联系越不明确。
2.2.2 封堵PFO是否有效
2000年Wilmshurst等首次发现封堵PFO可以减轻偏头痛症状或发作次数。此后,多项回顾性或单中心研究发现,封堵PFO可消除或减少头痛发作。2020年麻省总医院对110例PFO封堵术后偏头痛患者进行了3.2年的随访,发现封堵PFO后MA和MwoA患者的头痛症状均得到了显著改善,且MA患者头痛症状改善更好。研究证实术后有残余分流影响头痛症状的改善。
迄今为止,关于PFO封堵治疗偏头痛的3个随机对照实验(randomized controlled trial,RCT)(MIST、PRIMA和PREMIUM)研究,均没有明确证实封堵PFO对消除或减少偏头痛有显著获益,然而,封堵PFO可以使偏头痛完全缓解人数增加。一项meta分析纳入上述3个RCT研究,发现PFO封堵组偏头痛发作的平均次数显著减少(平均差异:−0.54;95%CI:−0.63-−0.45;P<0.01)、每月天数也显著减少(平均差异:−1.33;95%CI:−2.32-−0.33;P<0.01)。然而,两组患者在完全终止偏头痛发作方面没有显著差异。最新对使用Amplatzer PFO封堵器的PRIMA和PREMIUM研究进行的一项汇总分析表明,封堵PFO可使每月偏头痛天数显著减少(−3.1vs.−1.9,P=0.02),每月偏头痛发作次数(−2.0vs.−1.4,P=0.01)和偏头痛完全停止的患者数量增加[14(9%)vs.1(0.7%);P<0.001]。鉴于偏头痛是一个多因素疾病,单一治疗无法彻底解决偏头痛复发问题,以根治作为临床研究的终点事件过于理想化,这也是有些临床研究无法取得阳性结果的根源所在。
我国对封堵PFO治疗偏头痛亦进行了大量研究,单中心报道封堵PFO有效率与国外基本一致,吉林大学一项随访5年的研究发现,封堵PFO对长期缓解偏头痛有效。究竟哪些偏头痛封堵PFO获益多,国人发现持续性RLS、对抗血小板药物敏感及MA等为预测因素。但应注意,封堵PFO也偶尔引起或加重偏头痛。
【推荐意见】
①推荐偏头痛患者,首先使用偏头痛常规药物治疗(1A)。②偏头痛患者,合并缺血性脑血管病/难治性偏头痛/易栓倾向,应进行PFO筛查(1B)。③推荐偏头痛患者,合并PFO-AS,应选择PFO封堵治疗(1A)。④对于未能从常规药物治疗中获益的难治性偏头痛患者,未发现其他偏头痛发病机制,如果有先兆症状/ASA/持续性RLS或中-大量RLS/易栓倾向,相关学科综合评估认为PFO封堵的不确定获益较高,风险较低,建议选择PFO封堵治疗(2C)。
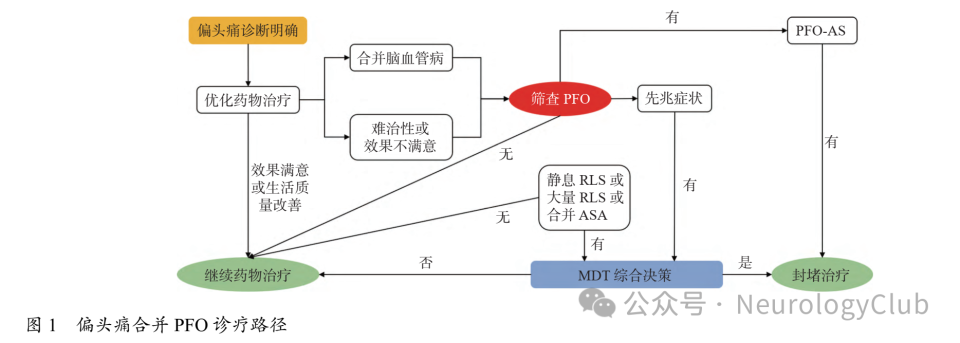
偏头痛合并PFO诊疗路径,见图1。

03
减压病
减压病(decompression sickness,DCS)是指机体从高压环境骤然转至低压环境时,体内原已溶解的气体(主要是氮气)超过了过饱和界限,在血液和组织中形成气泡,从而导致全身多个器官和部位,如皮肤、关节、骨骼、心血管系统、神经系统等的损伤。其严重程度取决于体内气泡的体积、数量、所在部位和持续时间等。临床表现复杂而多变,可表现为脉搏增快,皮肤粘膜发绀、关节疼痛等,也可表现为肺栓塞或肺水肿,严重者可导致神经系统损伤、瘫痪、休克以致死亡。DCS最常见于潜水作业、沉箱作业、开挖隧道的工人群体,以及特殊飞行史、非增压座舱式飞机驾驶员等。商用飞机飞行员DCS的风险可以忽略不计。
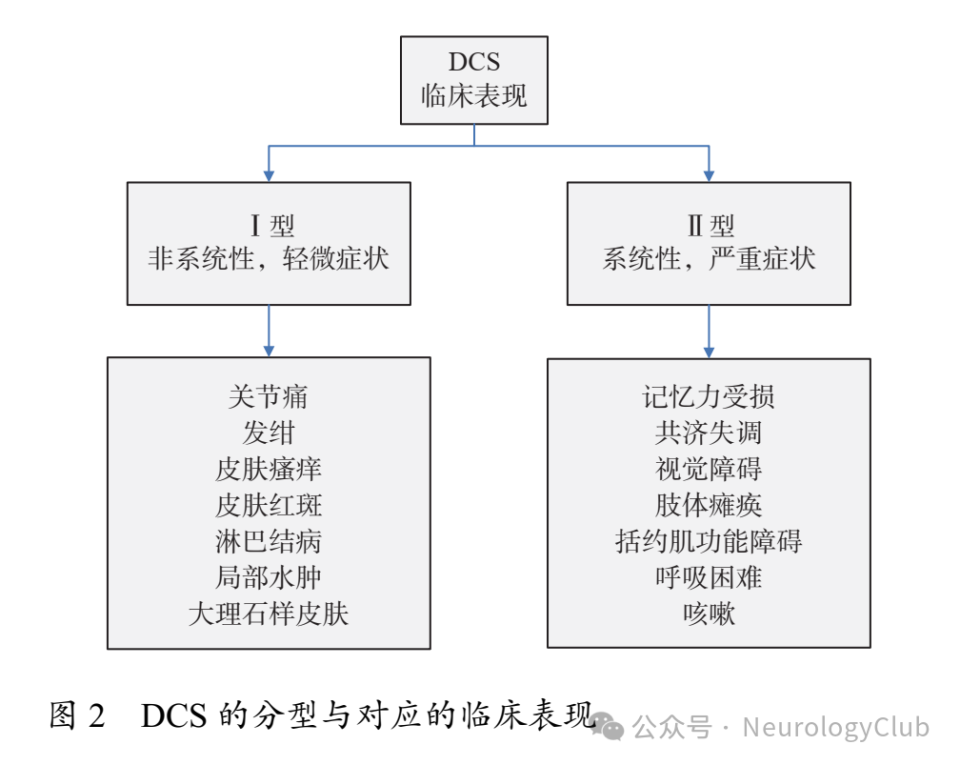
目前,DCS主要分为以下两种病理生理状态,其各自的临床表现概述如图2。伴有PFO的DCS具有早期出现症状、神经或皮肤损害为主、易再发的特点。
3.1 PFO引起DCS的机制
减压不当可能引起DCS,而PFO的存在,则增加了潜水员发生DCS的风险。潜水者按照规范的减压流程进行上浮,由于环境压力下降,可能在其静脉系统内出现气泡,大多数情况下,这些气泡可以被肺组织过滤。个别情况下,当静脉循环中存在大量气体栓子时,可能会出现剧烈而严重的症状,例如咳嗽、呼吸困难甚至肺水肿。当潜水者体内存在PFO时,则有可能由RLS而出现动脉气体栓塞,影响中枢神经系统。
伴有持续开放PFO的潜水员,生理条件下就会产生RLS。潜水时平衡中耳压力,长时间的Valsalva动作也会迅速增加右心房压力;以及氮气气泡引起的肺栓塞,可导致肺血管阻力增加和右心房压力增加,使得PFO开放,RLS增加。同时一些呼吸道的演习如深海潜水已被证明可改变胸内压力,一过性改变心房内压力阶差。
3.2 PFO与DCS的争议
3.2.1 是否可评估PFO和DCS的因果关系?
从现有的循证数据来看,多数的病例对照研究、小样本注册研究、病例报道和动物实验均支持PFO是引发DCS的一个重要因素,也有部分临床观察性研究或荟萃分析的结果不支持PFO引发DCS的证据。
现有的调查数据显示,潜水过程中,DCS的患病概率较低,波动于0.01%-0.095%之间,但若体内存在PFO,其DCS的发病率可增加2.5至5倍。存在PFO的潜水员在其罹患DCS时,临床损害最常出现的部位是大脑,而不是脊髓,氮气泡更易迁移到颈动脉和椎动脉。最近欧洲共识的meta分析发现,与没有DCS的受试者相比,DCS患者的RLS的优势比为5.63(95%CI:3.14-10.09)。
大的PFO更有可能与DCS有因果关系。Honěk等最近进行的一项研究证实,在专业水肺潜水员中,存在3级分流的PFO的存在与无明确诱因的DCS发作显著相关。PFO大小也是DCS复发的预测因子。对于有过DCS史的潜水员而言,其体内PFO越大,越容易再次发生DCS。
3.2.2 合并PFO的DCS是否需要封堵?
尽管研究发现封堵高危PFO,可以完全消除模拟潜水动脉循环中的气泡,是预防DCS的一种可行方法,但仍不建议将PFO封堵术作为一级预防策略。
对于合并PFO的DCS患者,可以选择停止潜水活动、减少潜水时间和深度及PFO封堵术三种方法进行二级预防。保守潜水可使大PFO潜水员的DCS风险明显降低。一项105例有DCS或高危PFO病史的潜水员接受了封堵治疗,其中绝大多数人恢复了非限制性潜水。DIVE-PFO登记系统的长期研究结果发现,随访7.1年PFO封堵组无一例发生DCS,保守治疗组有11例发生至少1次DCS。尽管DIVE-PFO登记研究存在选择偏倚,但导管疗法比传统疗法更有效。封堵是否完全也与DCS的复发风险有关,研究报道[56]59例有DCS病史的潜水员中,4例名封堵术后DCS复发,其中3例有残余分流。因此,强调完全关闭(无分流)的必要性,否则应避免无限制潜水。
由于缺乏大规模RCT,现有的证据的研究质量较低。最近发表的欧美共识,仍不建议将PFO封堵术作为首选解决方案。
【推荐意见】
①推荐对于已经发生DCS的患者,首先应通过改变生活方式、按照规定减压、减少潜水次数和潜水前吸入高浓度氧气等措施,降低减压事件的发生风险(1B)。②不建议对潜水员进行PFO普遍性筛查(2B)。③建议对于既往有偏头痛或隐源性卒中等病史,有ASD家族史,有DCS病史,且潜水频率非常高的潜水员,进行PFO筛查(2C)。④对于有过DCS病史,排除了其他危险因素,高度怀疑DCS与PFO相关,不愿意停止潜水并改变DCS危险因素的患者,建议可以考虑经导管封堵PFO(2C)。⑤建议经影像学证实PFO封堵后完全无残余分流的潜水员,才能恢复无限制潜水,否则只能进行一些低风险的潜水等行动(2B)。
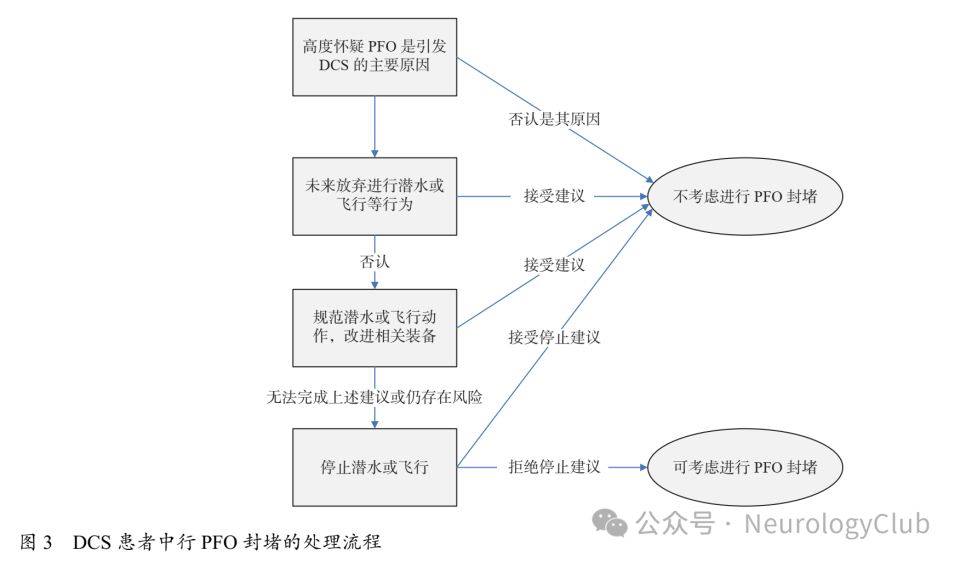
总之,DCS被认为是潜水员最常见的疾病之一。虽然近期的研究让PFO在其病理生理学中的作用得到了更好的解释。但对于存在PFO潜水员的日常医疗保健,无论是选择保守治疗还是PFO介入治疗,都应基于医学专家、潜水专家和患者本人共同的决策。未来也需组织更大的随机对照临床研究,以阐明DCS的最佳预防和治疗方法。对于DCS患者的PFO应对流程见图3。

04
斜卧呼吸-直立性低氧血症
斜卧呼吸-直立性低氧血症(platypnea-orthod-eoxia syndrome,POS)是指以体位性低氧血症伴有呼吸困难为特征的罕见综合征,其特点为立位时气短明显加重,动脉血氧饱和度及氧分压明显下降,而卧位时明显缓解。POS多见于老年人和女性,其患病率尚不清楚。
POS病因不清楚,主要由心内分流、肺动静脉分流及肺内通气/灌注不匹配三种原因引起。任何引起肺动静脉分流的疾病都可能与POS有关,导致低氧血液从肺动脉向肺静脉发生RLS。如肺动静脉畸形或肝肺综合征。动静脉瘘通常位于肺基底部,血液从肺动脉向肺静脉发生右向左分流引起缺氧。在直立位时,这些区域的流量增加,因此分流增加。在肝肺综合征患者中,肺毛细血管和毛细血管前血管的扩张决定了通气-灌注不匹配、动静脉肺分流和肺泡-动脉氧弥散减少。立位缺氧与直立时肺内血管扩张的优先灌注有关。心内分流引起POS最多见,最常见于PFO,也可见于ASD。
4.1 PFO引起POS的机制
尽管POS的确切发病机制不清楚,但临床发现大多数POS患者合并PFO或ASD,且封堵PFO后可明显改善症状。因此,房间隔结构异常可能是POS发生的基本病理基础。通常情况下右心房压力小于左心房压力,存在PFO或ASD亦很少有RLS,不会引起低氧血症。即使吸气、咳嗽、憋气及做Valsalva动作时,短暂的右房压力大于左房压,引起明显的RLS,也较少引起低氧血症。POS直立位时经PFO的RLS较卧位时大,同时需有许多加权因素共同作用,才能引起明显低氧血症,是一个非常复杂的病理生理过程。文献报道,引起POS的PFO需具有高危特征,同时合并其他病变的可能机制有:
4.1.1 心房压力梯度的变化
当右心房压力高于左心房压力时,可通过PFO或ASD发生RLS,通常与右心室顺应性降低相关。可见于肺栓塞、心脏压塞、缩窄性心包炎、右心室心肌梗死、年龄相关性右心室僵硬、气胸和肺切除术后急性促发、引起慢性肺动脉高压或重度三尖瓣反流的任何慢性疾病、右心房黏液瘤或嗜酸细胞增多性心内膜心肌病(或称Loeffler心内膜谈)等。
4.1.2 血流“优先”理论
没有右心房高压,直立状态时房间隔水平扭曲,房间隔与下腔静脉关系改变,血流优先从下腔静脉直接流向PFO,从右心房分流至左心房发生RLS,形成POS。可见于升主动脉扩张、胸椎后侧凸或右膈肌麻痹、持续的欧式瓣或Chiari网及房间隔下段脂肪性肥厚等。此外,升主动脉扩张会导致右心房顺应性降低,房间隔和下腔静脉之间的角度变窄,更有利于静脉血流回流到缺损处。
肺切除术和肺部手术是最早与POS相关的疾病,两种机制均可发挥作用。此外,POS多见于老年人,与随着年龄的变化,右心房和左心房之间相互的顺应性关系发生生理学的变化,使得右心房比左心房顺应性差,RLS增多有关。
4.2 PFO合并POS是否需要封堵?
封堵PFO改善POS缺氧的报告多来自个案报道。Mojadidi等对17例PFO伴有POS者实施了PFO封堵术,术后11例患者呼吸困难和低氧血症得到改善或完全缓解(无缓解者缺氧主要由肺部原因引起)。2016年Shah等对单中心52例POS合并PFO且进行介入治疗的患者进行回顾性分析发现,封堵术后,所有患者氧饱和度都有明显改善。应注意的是,POS患者伴发疾病往往都很严重,除了治疗POS外,应重视伴随疾病的治疗。
【推荐意见】
①推荐POS患者进行PFO筛查(1C);②关闭PFO之前,推荐常规进行标准化右心导管检查,明确PFO和POS的临床相关性(1C)。③对于POS,既往无PFO-AS且已排除其他缺氧原因的患者,建议关闭PFO(2C)。

05
外周(非脑血管)栓塞
反常栓塞不仅引起卒中,而且也引起心肌梗死(myocardial infarction,MI)、急性肢体缺血、肾梗死、脾梗死或肠系膜梗死等非脑血管周围栓塞(noncerebrovascular peripheral embolism,NCPE)。由于主动脉弓的解剖特点,血流易对大脑血管造成影响,较少影响外周血管,加之大脑对缺血更加敏感。因此,反常栓塞多关注脑血管事件,而对NCPE认识不足。
NCPE最常见的部位是四肢和冠状动脉,而肾、脾和肠系膜动脉罕见。据报道2%的四肢动脉栓塞与反常栓塞有关。反常栓塞引起的MI不足1%,但根据全球每年约700万例MI估计,每年PFO反常栓塞引起的MI至少35,000例。估算反常栓塞引起MI发生率为10例/100万人。
与PFO-AS一样,反常栓塞引起NCPE主要是一个排他性诊断。2007年Rigatelli等提出了颅外反常栓塞的诊断标准,分为主要标准和次要标准。主要标准包括:有PFO/筛状ASA(可伴ASD)、心脏超声检查提示分流存在、cTCD提示分流呈淋雨或帘状、ST段抬高型MI或非ST段抬高型急性冠脉综合征(冠状动脉正常)或临床相关的外周缺血证据(超声证实既往无动脉疾患)。次要标准包括:有MA病史、MRI提示有脑缺血发作病灶、现在或过去为高凝状态。
封堵PFO预防NCPE复发,主要借鉴预防PFO-AS的复发。PC试验虽也纳入了NCPE患者,但仅占研究人群的2.6%(11例),无法就该亚组得出任何结论。最近一项多中心研究,比较了1136例发生血栓栓塞事件后接受PFO封堵术的连续患者,其中脑血管事件1,099例(96.7%)、NCPE37例(3.3%),中位随访时间为3年。发现接受PFO封堵术的NCPE事件患者,其远期结果与脑血管事件相似,血栓栓塞事件的复发率非常低。
【推荐意见】
对于既往无PFO-AS,且临床排除其他栓塞病因的NCPE患者,发现PFO伴有ASA/持续性RLS或中-大量RLS,推荐关闭PFO(1C)。

06
静脉血栓栓塞症
静脉血栓栓塞症(venous thromboembolism,VTE)包括深静脉血栓形成和肺血栓栓塞症。遗传性或获得性血栓形成倾向与较高的静脉血栓栓塞和缺血性卒中风险相关。高凝状态合并PFO并不罕见,患病率为5%-31%,同时存在这两种情况可能会增加卒中风险。然而,有关PFO与隐源性卒中的RCT研究,基本上排除了许多有血栓形成倾向的潜在高危患者,无法根据前瞻性数据评估其卒中发生率和PFO封堵术的潜在保护作用。最近Buber等回顾性研究了136例PFO合并高凝状态患者,发现与接受抗凝或抗血小板治疗药物比较,PFO封堵合并抗凝治疗可使高凝状态患者脑血管意外或短暂性脑缺血发作风险显著降低,但其房颤和其他严重不良事件的风险也增加。支持在高凝状态的高危患者人群中,至少应该考虑PFO封堵术。
【推荐意见】
①对于有深静脉血栓形成病史且既往无PFOAS的患者,不建议在抗栓治疗的同时关闭PFO(2C)。②对于有血栓形成倾向且既往无PFO-AS的患者,不建议在抗栓治疗的同时关闭PFO(2C)。③对于有深静脉血栓形成或肺血栓栓塞症病史,有反常栓塞发作的患者,推荐抗凝治疗的同时关闭PFO(1C)。

07
偶然发现PFO
在健康体检等检查时炒股资金配资,常偶然发现PFO,特别是PFO合并ASA、持续RLS或大量RLS,告知这类人群为高危PFO,将引起一定的恐惧或心理负担。目前尚缺乏关于封堵解剖学上高危无症状PFO人群潜在益处的相关报道。这一人群中,PFO关闭的益处非常不确定,需要进一步的研究来确定这一种人群是否会从关闭中受益。
天莹网提示:文章来自网络,不代表本站观点。



